سهشنبه 17 فروردین 1400 کد خبر: 91

۱-مقدمه
به دلیل فرایند صنعتی شدن در سالهای اخیر؛ خاک، یکی از با ارزشترین بخشهای طبیعت، به سرعت در حال آلوده شدن است. دفع مواد شیمیایی زبالههای صنعتی به خاک، استفاده بدون کنترل از کود، آفتکشها و دیگر مواد شیمیایی کشاورزی باعث آلودگی خاک شدهاند. مهمترین آلایندههای خاک عبارتند از فلزات سنگین، شبهفلزات، فراوردههای نفتی و آفتکشها[۱].
شکل ۱ آلایندههای خاک در سال ۲۰۱۱ در اروپا را نشان میدهد که طبق آن ۳۷/۳ درصد آلایندههای خاک، فلزات سنگین میباشند[۲]. خاکهای آلوده سلامت انسان، اکوسیستم، کشاورزی و بطور کلی محیط را تحت تاثیر قرار میدهد.

شکل۱- آلاینده های موجود در خاک و آب های زیرزمینی[۱]
بنابراین پاکسازی خاکهای آلوده تبدیل به مسئله مهمی در فناوریهای زیست محیطی شدهاست. دراین مقاله به روشهای پاکسازی این آلایندهها و همچنین نقش فناوری نانو در این حوزه خواهیم پرداخت.
۲-انواع روشهای تصفیه خاک
در این بخش به طور خلاصه به روشهای مختلفی که برای پاکسازی خاک وجود دارد خواهیم پرداخت.
۱-۲- تصفیه فیزیکی[۱]
تصفیه فیزیکی به طور کلی شامل روشهای جایگزینی خاک[۲] و واجذب حرارتی[۳] است. در روش جایگزینی خاک، خاک آلوده یا بخشی از آن با خاک سالم جایگزین میشود. در روش واجذب حرارتی، خاک توسط امواج یا حرارت مستقیم گرم میشود تا آلایندهها فرّار و ناپایدار شوند. سپس آلایندهها از طریق حامل گازی به بیرون منتقل میشوند. این روش عمدتا برای فلزات سنگین مانند جیوه و آرسنیک استفاده میشود[۳].
۲-۲- تصفیه شیمیایی[۴]
تصفیه شیمیایی شامل شستشوی شیمیایی[۵]، پایدارسازی[۶] و تصفیه الکتروکینتیک[۷] میشود. در روش شستشو، خاک آلوده توسط آب، واکنشگرها یا گاز شسته شده و آلاینده از خاک خارج میگردد[۴]. در روش پایدارسازی، موادی به خاک افزوده میشوند و از طریق واکنش با آلایندهها آنها را به مواد نامحلول یا ثابت و بیتحرک تبدیل میکنند. همچنین این افزودنیها قابلیت کاهش سمیت و تحرکپذیری فلزات سنگین را داشته و مانع ورود آنها به آب، گیاهان و سایر بخشهای محیط میشود[۵]. در روش الکتروکینتیک، دو الکترود به خاک وارد میشوند و به آنها اختلاف پتانسیل اعمال میشود؛ در نتیجه میدان الکتریکی تشکیل شده باعث حرکت آلایندهها به سمت الکترودها و خنثی شدن بار الکتریکی آنها میشود که کاهش سمیت آلایندهها را به دنبال دارد[۶].
۳-۲- تصفیه زیستی
در تصفیه زیستی از گیاهان زنده برای جذب آلایندهها و پاکسازی محیط خاک استفاده میشود. همچنین از میکروارگانیسمها برای جلوگیری از حرکت آلایندهها درون خاک استفاده میشود.
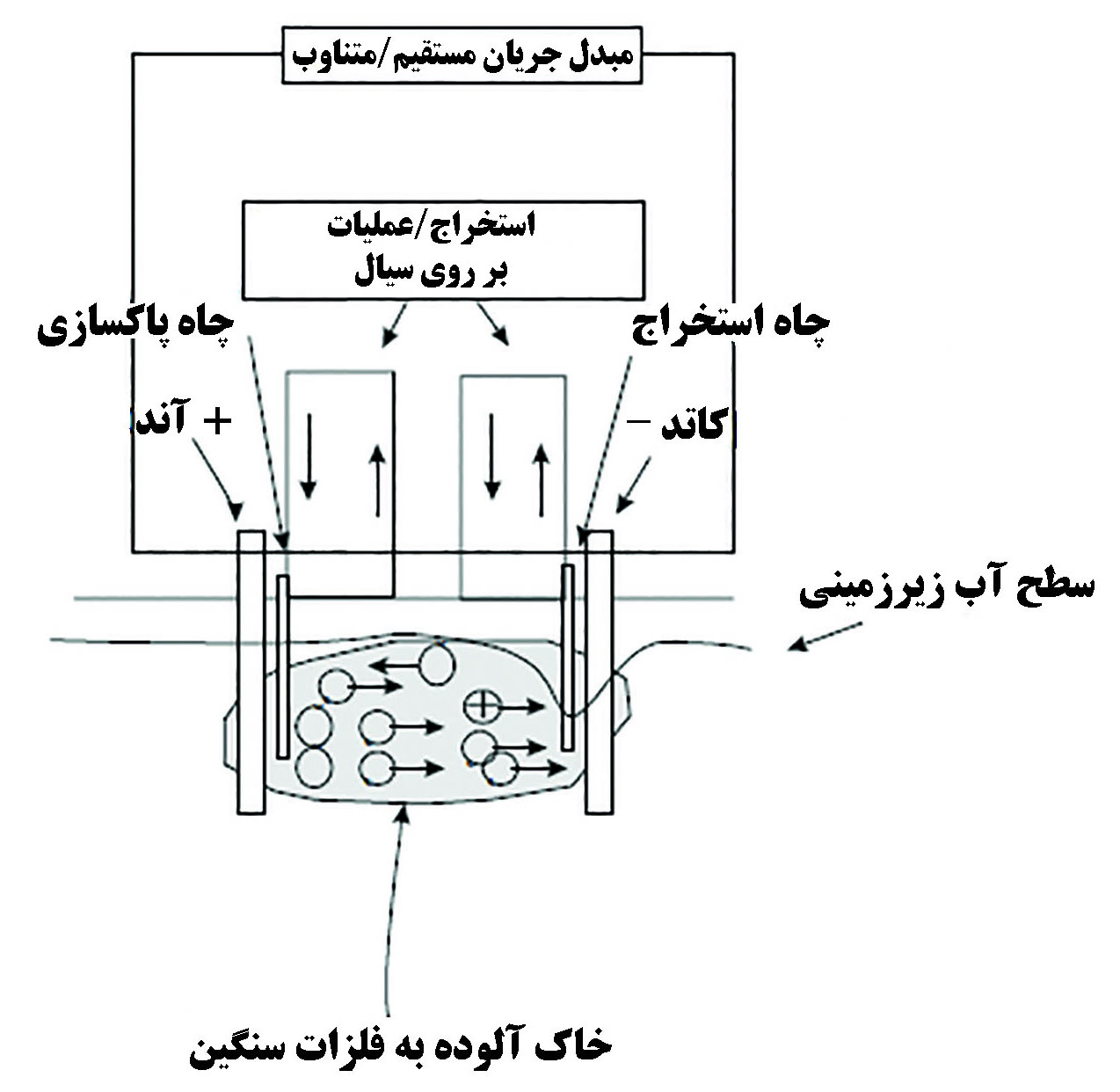
شکل۲- روش الکتروکینتیک [۴]
۳- فناوری نانو و کاربرد آن در تصفیه خاک
علوم و فناوری نانو با استفاده از مواد در ابعاد ۱ تا ۱۰۰ نانومتر به حل چالشهای فناورانه موجود میپردازد. نانومواد با ابعاد کوچک و شکلهای متنوع، سطح بسیار زیاد و مکانهای واکنش[۸] بسیاری دارند که باعث تمایل بالای آنها برای واکنش، جذب و فعالیتهای کاتالیستی میشود. در سالهای اخیر، فناوری نانو در حوزه محیط زیست به منظور تصفیه آب و پساب، هوا، خاک و ... توجه دانشمندان را به خود جلب کردهاست. روشهای تصفیه برپایه فناوری نانو موثر و کم هزینه بوده و آسیبی به محیط زیست وارد نمیکنند. در طول فرایند گندزایی، اغلب برهمکنشها در سطح مشترک مابین نانومواد و آلاینده اتفاق میافتد. از آنجایی که سطح ویژهی نانومواد بسیار زیاد است، این برهمکنشها با سرعت بالایی رخ میدهند و وجود تعداد زیاد سایتهای فعال، باعث افزایش نرخ تصفیه و افزایش بازده گندزدایی میشود. همچنین اندازه کوچک نانوذرات به نفوذ راحت و سریع آنها به نواحی آلوده شده کمک میکند. نانوذرات، با توجه به کاربرد و عملکردشان، میتوانند اصلاح سطحی یا ساختاری شوند و بازده و کیفیت گندزدایی را بهبود بخشند. این دسته از نانو مواد نه تنها در تصفیه آلایندهها، بلکه در تشخیص آنها کاربرد دارند. تمامی خواص یاد شده، نانومواد را به گزینه مناسبی برای استفاده از آنها در تصفیه آلایندهها تبدیل کردهاست[۷].
در نواحی مختلف جهان، به منظور تصفیه خاک، از روشهای در محل[۹] و خارج از محل[۱۰] استفاده میشود. میتوان محلول کلوئیدی یا آبی نانوذرات را از طریق اسپریکردن یا تزریق به کمک گرانش یا فشار به خاک آلوده وارد کرد. هنگامی که نانومواد به خاک تزریق میگردند، یک ناحیهی پاکسازی[۱۱] تشکیل داده و در سوسپانسیون باقی میمانند[۸].
۴- انواع آلایندههای خاک و کاربرد فناوری نانو در تصفیه آنها
۱-۴- فلزات سنگین
فلزات سنگین اصلیترین آلایندههای خاک هستند و از این رو، پاکسازی آنها از اهمیت بالایی برخوردار است. دسته بزرگی از فلزات و همچنین شبهفلزات در گروه فلزات سنگین قرار میگیرند. برجسته ترین فلزات سنگین که برای محیط زیست و سلامت انسان تهدید به شمار میروند عبارتند از: آرسنیک، سرب، کادمیوم، کروم، مس، جیوه، نیکل و ... . این دسته از آلایندهها را می توان به کمک نانوذرات به طور موثری از خاک پاکسازی کرد[۹-۱۱]. در این بخش به کاربرد فناوری نانو در تصفیه خاکهای آلوده به فلزات سنگین خواهیم پرداخت.
تکنیکهای زیست سازگاری که به منظور پاکسازی فلزات سنگین از خاک استفاده میشوند، عبارتند از جذب[۱۲] آلایندهها و پایدارسازی[۱۳] آنها[۱۲]. بطور کلی مواد مورد استفاده در تصفیه خاک بر اساس تکنیک پاکسازی به دو دسته جاذب[۱۴] و واکنشگر[۱۵] تقسیم میشوند. مواد جاذب، آلایندهها را از طریق جذب آلاینده بر روی سطح بیرونی یا ساختار درونی از محیط حذف میکنند. همچنین تکنیک جذب یکی از بهترین روشهای پاکسازی فلزات سنگین از خاک میباشد زیرا ساده، ارزان و دارای بازده بالا میباشد. این روش برای حذف یونهای فلزاتی مانند مس، جیوه، کادمیوم و کروم استفاده میشود. ظرفیت جذب، به ماده مورد استفاده بستگی دارد. اندازه کوچک و مساحت سطح بالای نانومواد باعث شده تا ظرفیت و سرعت جذب آنها بسیار افزایش یابد[۱۳]. از سوی دیگر، مواد واکنشگر از طریق واکنشهای شیمیایی مانند اسید- باز، ردوکس، رسوب دهی، تبادل یونی و واکنشهای فوتوکاتالیستی آلایندهها را از بین میبرند[۱]. در طی فرایند گندزدایی، مواد سمی به سرعت تبدیل به موادی با سمیت به مراتب کمتر میشوند. براساس پژوهشهای انجام شده، نانوذرات متنوعی برای تصفیه آبهای آلوده شده با مواد فلزی مورد استفاده قرار میگیرند. اما مواد گزارش شده برای پاکسازی فلزات سنگین از خاک محدود هستند. همچنین اغلب مطالعات انجام شده بر روی خاک های آلوده به فلزات سنگین در مقیاس آزمایشگاهی هستند و پژوهشهای عملی و میدانی کمتری گزارش شدهاند. در ادامه، پرکاربردترین نانوموادی که برای تصفیه خاکهای آلوده به فلزات سنگین استفاده شده اند را بررسی میکنیم.
روشهای تصفیه بر پایه آهن به سرعت در حال رشد بوده و در مقیاسهای مختلف آزمایشگاهی و صنعتی در حال آزمایش هستند[۱۴]. مزیت اصلی آهن، این است که در دسترسترین فلز موجود بر روی زمین میباشد و جاذبهای تهیه شده از این فلز، بسیار به صرفه میباشند. بعلاوه آهن غیرسمی است و از این رو دوستدار محیط زیست است. نانوذرات آهن صفر ظرفیتی[۱۶]، اندازه بسیار کوچکی دارند که به آنها کمک میکند به مناطق آلوده نفوذ کنند. همانطور که در بخش قبل هم ذکر شد، به دلیل مساحت سطح بالای نانوذرات، سطح تماس آنها با آلایندهها افزایش یافته و بازده گندزدایی نسبت به ماده در حالت توده بهبود مییابد. نانوذرات آهن در کلوئیدها پایداری خوبی دارند پس می توان آنها را مستقیما به خاک، رسوبات و سفرههای آب زیرزمینی تزریق نمود. همچنین این نانوذرات خواص جذب و احیای مناسبی دارند که باعث می شود با فلزات سنگینی از قبیل جیوه، نیکل و کادمیوم واکنش دهند. این نانوذرات در برابر خوردگی مقاوم هستند و در شرایط مختلف قادر به تغییر ظرفیت خود میباشند. خواص ذکر شده، نانوذرات آهن صفر ظرفیتی را به یکی از بهترین گندزداهای خاک تبدیل کردهاست[1,15]. نانوذرات صفر ظرفیتی آهن به وفور برای حذف جیوه ()، نیکل ()، کادمیوم()، سرب() و کروم () استفاده میشوند[۱,۱۱]. مکانیزم اصلی تصفیه فلزات سنگین، جذب و احیای آنها به یونهایی با ظرفیت و سمیت کمتر و پایدارسازی آنها میباشد[۱۵]. واکنش انجام شده بین نانوذرات آهن و فلز سنگین، به پتانسیل استاندارد الکترود (E0) فلز وابسته است. فلزات سنگینی مانند کادمیوم و روی، پتانسیل استاندارد منفیتری نسبت به آهن صفرظرفیتی دارند و روی پوسته آهن جذب میشوند. از طرفی، برخی فلزات مانند کروم، آرسنیک و مس با پتانسیل استاندارد الکترود مثبتتر از آهن، احیا میشوند و در خاک رسوب میکنند.
فلزات سنگینسرب و نیکل با پتانسیل استاندارد کمی مثبت تر از آهن، احیا میشوند و سپس توسط نانوذرات آهن صفرظرفیتی جذب میگردند. در شکل ۳ یک ساختار هسته پوسته نانوذره آهن صفر ظرفیتی نشان دادهشده و مکانیزم تخریب آلاینده را نشان میدهد[۳].
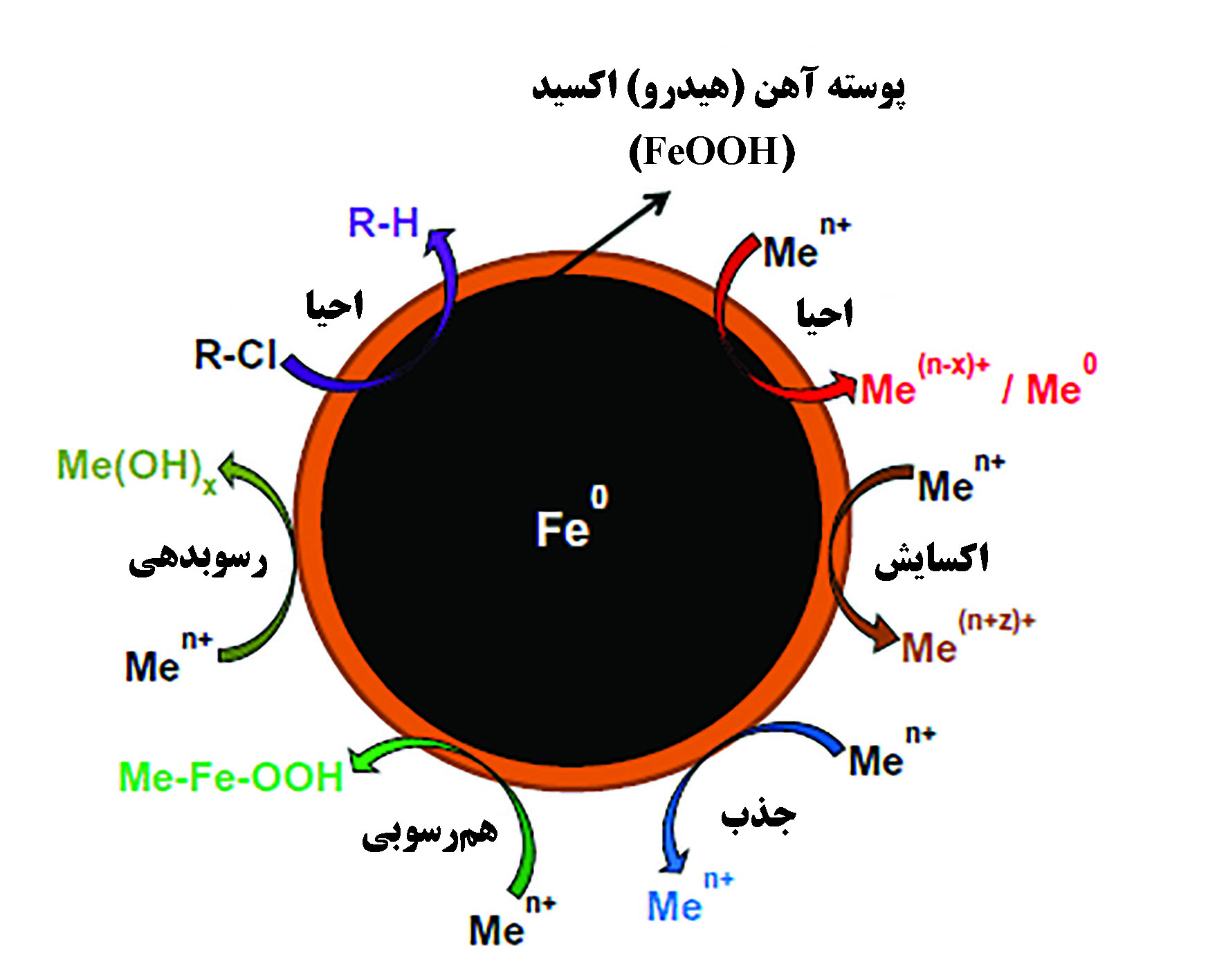
شکل۳- نانوذره هسته پوسته آهن صفر ظرفیتی و مکانیزم های تخریب آلاینده [۳]
مهمترین ضعف نانوذرات صفرظرفیتی آهن، این است که به علت سطح زیاد، به سرعت اکسید میشوند. بنابراین هر ذره آهن، دارای یکلایه نازک اکسیدآهن است که با گذر زمان، ضخامت این لایه افزایش مییابد و فعالیت گندزدایی آهن کاهش مییابد؛ اگرچه این لایه اجازه عبور الکترونها از هسته به خارج نانوذره را میدهد و کمک میکند تا نانوذره آهن خاصیت کاهندگی خود را حفظ کند. همچنین وجود این لایه اکسیدی باعث میشود نانوذرات آهن صفرظرفیتی بتوانند با ترکیبات آلی نیز واکنش داده و آلایندههای آلی را تخریبکنند. به منظور کاهش نرخ اکسیدشوندگی، نانوذرات آهن توسط برخی اکسیدهای فلزی یا فلزات نجیب پوشش داده میشوند[۱۵]. افزودن مقادیر بسیار کم فلزی دیگر به ساختار نانوذرات آهن(دوپ کردن[۱۷])، باعث افزایش چشمگیری در واکنشپذیری آنها میشود؛ زیرا فلز ثانویه مانند یک کاتالیست عمل کرده و فعالیت گندزدایی نانوذرات آهن را بهبود میبخشد؛ پالادیوم، رایجترین ذره برای این فرایند است. نانوذرات آهن تمایل زیادی برای تجمع و کلوخهای شدن نشان میدهند که باعث محدودیت کاربری آنها میشود. به منظور جلوگیری از کلوخهای شدن این ذرات و افزایش تحرک و قابلیت انتقال آنها، انواع مختلفی از اصلاح سطحی روی آنها صورت میگیرد. این اصلاح سطحی معمولا از طریق افزودن یک ماده پلیمری یا سورفکتانت و ایجاد دافعه فضایی میباشد و این کار باعث افزایش پایداری نانوذرات در محیط میشود. در یک پژوهش از نانوذرات صفرظرفیتی آهن پایدارشده با کربوکسیمتیلسلولز برای حذف کادمیوم استفاده شده و مشاهده گردید که پایداری نانوذرات در کلوئید و نفوذ آنها بهبود یافته و این باعث افزایش جذب کادمیوم نسبت به حالت اصلاح نشده میگردد[۱۶]. در پژوهشی دیگر با استفاده از روش الکتروکینتیک و سد فعال نفوذپذیر[۱۸] پر شده با نانوذرات صفر ظرفیتی آهن، کروم شش ظرفیتی با بازده ۸۸درصد به کروم سه ظرفیتی تبدیل شد. مکانیزم EK/PBR، شامل واکنش احیا و به طور همزمان فرایند جذب-واجذب میباشد. افزودن نانوذرات آهن صفرظرفیتی به این مکانیزم، به جذب و احیای یونهای کروم کمک میکند[۱۷].
نانوذرات آهن صفرظرفیتی برای اولین بار در سال ۱۹۹۷ با استفاده از احیای توسط NaBr سنتز شدند [۱۸]. اما این روش تنها برای کاربرد آزمایشگاهی استفاده میشود؛ زیرا این روش سنتز، هزینه بالایی دارد (بیش از ۲۰۰ دلار بر کیلوگرم). روش دیگر تهیه نانوذرات آهن صفرظرفیتی احیای پنتاکربونیل آهن(Fe(CO)5) در آرگون و آمونیاک میباشد[۱۹]. اما به دلیل سمیت بالای فراوردههای تولید شده، این روش نیز مناسب نمیباشد. روش صنعتی تهیه این نانوذرات احیای FeOOH یا Fe2O3 توسط گاز هیدروژن در دمای بالا میباشد[۲۰].
تزریق مستقیم نانوذرات به خاک و آبهای زیرزمینی نگرانیهای مربوط به سمیت نانوذرات و اثر آنها بر روی محیط زیست را مطرح کرده است اگرچه فواید آنها در گندزدایی و از بین بردن انواع آلایندهها مورد بررسی قرار گرفتهاست[۲۱]. اما درباره نانوذرات آهن صفرظرفیتی، سمیت ناشی از خود ذرات به ندرت گزارش شدهاست. در پژوهشی نشان داده شده است که به هنگام تزریق نانوذرات به خاک یا آبهای زیرزمینی، سمیت کمتری نسبت به آزمایشگاه مشاهده میشود؛ زیرا سرعت اکسید شدن در محیط بالاتر از سرعت اکسیداسیون در آزمایشگاه است[۲۲]. همچنین گزارش شده نانوذرات صفرظرفیتی آهن خود سمیت ندارند؛ اما می توانند ذرات سمی را جذب کرده و کیلومترها با خود حمل کنند[۲۳].
نانوذرات صفرظرفیتی آهن نه تنها در تصفیه خاکهای آلوده به فلزات سنگین بلکه در تصفیه آلایندههای آلی و آنیونهای غیرآلی نیز نقش مهمی دارند. انواع مواد قابل تصفیه و حذف توسط نانوذرات آهن صفرظرفیتی عبارتند از:
نانوذرات سولفیدآهن گزینه مناسبی برای حذف جیوه از خاک میباشند. پژوهشها نشان داده اند نانوذرات سولفید آهن پایدار شده با کربوکسیمتیلسلولز(CMC) توانایی بالایی در حرکت در خاک و همچنین حذف جیوه از طریق جذب، رسوبدهی و پایدارسازی از خود نشان میدهند[۲۴].
با اینکه تصفیه فلزات سنگین به کمک مواد فسفاته مانند فسفریکاسید و سنگهای طبیعی فسفات گزارش شدهاند، خواص فیزیکی و شیمیایی فسفات، کاربرد آنها در عمل را دچار محدودیت کردهاست. با توجه به اینکه آهن فلزی ارزان و غیرسمی است و به وفور درطبیعت یافت میشود، میتواند محدودیتهای فسفات را برطرف کند. نانوذرات فسفات آهن خطرات ثانویه محیط زیستی را به دنبال ندارند و بنابراین میتوانند جایگزین مناسبی برای سایر مواد فسفاته باشند. این نانوذرات معمولا برای حذف مس از خاک استفاده میشوند[۲۵].
نانوذرات اکسیدآهن جاذبهای قوی فلزات سنگین به شمار میروند. در صورت دوپ کردن زیرکونیوم در این ماده، پایداری آن افزایش یافته و همچنین قدرت جذب آن بیشتر میشود و برای حذف آرسنیک و سرب می توان از آن استفاده کرد[۲۶].
همچنین از آلوفان[۱۹] که ترکیب آبی آلومینوسیلیکات است برای جذب مس[۲۷] و از کربن بلک[۲۰] برای جذب روی و مس[۲۸] استفاده می شود.
۲-۴- نفت، فراوردههای نفتی و مواد آلی
آلودگیهای خاک ناشی از فراوردههای نفتی شامل بنزن، تولوئن، اتیلبنزن و زایلین (BTEX)[۲۱]، نگرانیهای زیادی را به وجود آوردهاند. از دیگر آلایندههای آلی مهم خاک میتوان به هیدروکربنهای آروماتیک پلی اکریلیک اشاره نمود(PAH)[۲۲].
رایجترین روشهای تصفیه این آلایندهها، استفاده از نانوذرات آهن صفرظرفیتی و همچنین مواد فوتوکاتالیست به منظور اشباع پیوندهای دوگانه و سهگانه، باز کردن حلقههای بنزنی و خنثیکردن پیوندهای ناقص میباشد. نانوذراتی از قبیل تیتانیومدیاکسید، اکسیدروی و اکسیدمس در صورت قرار گرفتن در معرض نور، میتوانند یک الکترون به لایه رسانش خود منتقل کنند و پیوندهای ناقص آلایندهها را برطرف کرده یا آنها را اشباع سازند[۲۹,۳۰].
۵- جمعبندی و نتیجهگیری
با گسترش صنایع و افزایش شهرنشینی، خاکها با سرعت بیشتری در حال آلوده شدن هستند. عمدهترین آلایندههای خاک فلزات سنگین و آلایندههای نفتی میباشند. روشهای قدیمی تصفیه خاک شامل روشهای فیزیکی، شیمیایی و زیستی هستند. با ظهور فناوری نانو، از روشهایی بهینه برای تصفیه خاک استفاده میشود. نانوذرات از طریق جذب و یا بیاثر کردن آلایندهها خاک را تصفیه می کنند. بارزترین نانوذرات مورد استفاده در تصفیه خاک نانوذرات آهن صفرظرفیتی، نانوذرات سولفیدآهن، اکسیدآهن و نانوذرات فوتوکاتالیست می باشند.
۶- منابع
[1] Caliman, Florentina, et al. “Soil and Groundwater Cleanup: Benefits and Limits of Emerging Technologies.” Clean Technologies and Environmental Policy, vol. 13, Apr. 2011, pp. 241–68, doi:10.1007/s10098-010-0319-z.
[2] Van Liedekerke, Marc, et al. “Progress in the Management of Contaminated Sites in Europe.” 2014, doi:10.13140/RG.2.1.4213.5444.
[3] Yao, Zhitong, et al. “Review on Remediation Technologies of Soil Contaminated by Heavy Metals.” Procedia Environmental Sciences, vol. 16, 2012, pp. 722–29, doi:https://doi.org/10.1016/j.proenv.2012.10.099.
[4] Tampouris, S., et al. “Removal of Contaminant Metals from Fine Grained Soils, Using Agglomeration, Chloride Solutions and Pile Leaching Techniques.” Journal of Hazardous Materials, vol. 84, July 2001, pp. 297–319, doi:10.1016/S0304-3894(01)00233-3.
[5] Yao, Zhitong, et al. “Review on Remediation Technologies of Soil Contaminated by Heavy Metals.” Procedia Environmental Sciences, vol. 16, 2012, pp. 722–29, doi:https://doi.org/10.1016/j.proenv.2012.10.099.
[6] Luo QS, Zhang XH, Wang H, et al. Mobilization of 2,4-dichlorophenol in soils by non-uniform electrokinetics. Acta Scientiae Circumstantiae, 2004; 24(6): 1104-9.
[7]Wei, Qiang, et al. “Applications of Nanomaterial-Based Membranes in Pollution Control.” Critical Reviews in Environmental Science and Technology, vol. 43, Jan. 2013, doi:10.1080/10643389.2012.672066.
[8] Watlington, Katherine. “Emerging Nanotechnologies for Site Remediation and Wastewater Treatment.” Report, US Environmental Protection Agency, Office of Solid Waste and Emergency Response, Office of Superfund Remediation and Technology Innovation, Technology Innovation and Field Services Division, Washington, DC, no. August, 2005, pp. 1–40, doi:10.2147/COPD.S34211 LK
[9] Al-Rashdi, Badriya, et al. “Heavy Metals Removal Using Adsorption and Nanofiltration Techniques.” Separation & Purification Reviews, vol. 40, no. 3, Taylor & Francis, Aug. 2011, pp. 209–59, doi:10.1080/15422119.2011.558165.
[10] Raymond A. Wuana and Felix E. Okieimen, “Heavy Metals in Contaminated Soils: A Review of Sources, Chemistry, Risks and Best Available Strategies for Remediation,” ISRN Ecology, vol. 2011, Article ID 402647, 20 pages, 2011.
[11] Li, Xiao-qin, et al. “Zero-Valent Iron Nanoparticles for Abatement of Environmental Pollutants: Materials and Engineering Aspects.” Critical Reviews in Solid State and Materials Sciences, vol. 31, no. 4, Taylor & Francis, Dec. 2006, pp. 111–22, doi:10.1080/10408430601057611.
[12] Almaroai, Yaser A., et al. “Natural and Synthesised Iron-Rich Amendments for As and Pb Immobilisation in Agricultural Soil.” Chemistry and Ecology, vol. 30, no. 3, Taylor & Francis, Apr. 2014, pp. 267–79, doi:10.1080/02757540.2013.861826.
[13] Shan, G, Yan, S, Tyagi, RD, Surampalli, RY & Zhang, TC 2009, 'Applications of nanomaterials in environmental science and engineering: Review', Practice Periodical of Hazardous, Toxic, and Radioactive Waste Management, vol. 13, no. 2, pp. 110-119.
[14] O’Carroll, Denis, et al. “Nanoscale Zero Valent Iron and Bimetallic Particles for Contaminated Site Remediation.” Advances in Water Resources, vol. 51, 2013, pp. 104–22, doi:https://doi.org/10.1016/j.advwatres.2012.02.005.
[15] Cundy, Andrew B., et al. “Use of Iron-Based Technologies in Contaminated Land and Groundwater Remediation: A Review.” Science of The Total Environment, vol. 400, no. 1, 2008, pp. 42–51, doi:https://doi.org/10.1016/j.scitotenv.2008.07.002.
[16] Nasiri, J., et al. “Removal of Cadmium from Soil Resources Using Stabilized Zero-Valent Iron Nanoparticles.” J. Civ. Eng. Urban., vol. 3, Jan. 2013, pp. 338–41.
[17] Shariatmadari, Nader, et al. “Enhancement of Hexavalent Chromium [Cr(VI)] Remediation from Clayey Soils by Electrokinetics Coupled with a Nano-Sized Zero-Valent Iron Barrier.” Environmental Engineering Science - ENVIRON ENG SCI, vol. 26, June 2009, pp. 1071–79, doi:10.1089/ees.2008.0257.
[18] Wang, Chuan-Bao, and Wei-xian Zhang. “Synthesizing Nanoscale Iron Particles for Rapid and Complete Dechlorination of TCE and PCBs.” Environmental Science & Technology, vol. 31, no. 7, American Chemical Society, July 1997, pp. 2154–56, doi:10.1021/es970039c.
[19] Karlsson, M. N. A., et al. “Size-Controlled Nanoparticles by Thermal Cracking of Iron Pentacarbonyl.” Applied Physics A, vol. 80, Apr. 2005, pp. 1579–83, doi:10.1007/s00339-004-2987-1.
[20] Liu, Haibo, et al. “Nitrate Reduction over Nanoscale Zero-Valent Iron Prepared by Hydrogen Reduction of Goethite.” Materials Chemistry and Physics, vol. 133, Mar. 2012, pp. 205–211, doi:10.1016/j.matchemphys.2012.01.008.
[21] Batley, Graeme E., et al. “Fate and Risks of Nanomaterials in Aquatic and Terrestrial Environments.” Accounts of Chemical Research, vol. 46, no. 3, American Chemical Society, Mar. 2013, pp. 854–62, doi:10.1021/ar2003368.
[22] Crane, R. A., and T. B. Scott. “Nanoscale Zero-Valent Iron: Future Prospects for an Emerging Water Treatment Technology.” Journal of Hazardous Materials, vol. 211–212, 2012, pp. 112–25, doi:https://doi.org/10.1016/j.jhazmat.2011.11.073.
[23] KARN, Barbara; KUIKEN, Todd and OTTO, Martha. Nanotechnology and in situ remediation: a review of the benefits and potential risks. Ciênc. saúde coletiva [online]. 2011, vol.16, n.1 [cited 2019-10-01], pp.165-178. [24] Gong, Yanyan, et al. “Immobilization of Mercury in Field Soil and Sediment Using Carboxymethyl Cellulose Stabilized Iron Sulfide Nanoparticles.” Nanotechnology, vol. 23, July 2012, p. 294007, doi:10.1088/0957-4484/23/29/294007.
[25] Liu, Ruiqiang, and Dongye Zhao. “In Situ Immobilization of Cu(II) in Soils Using a New Class of Iron Phosphate Nanoparticles.” Chemosphere, vol. 68, Sept. 2007, pp. 1867–76, doi:10.1016/j.chemosphere.2007.03.010. [26] Almaroai, Yaser A., et al. “Natural and Synthesised Iron-Rich Amendments for As and Pb Immobilisation in Agricultural Soil.” Chemistry and Ecology, vol. 30, no. 3, Taylor & Francis, Apr. 2014, pp. 267–79, doi:10.1080/02757540.2013.861826.
[27] Yuan, Guodong. “Natural and Modified Nanomaterials as Sorbents of Environmental Contaminants.” Journal of Environmental Science and Health, Part A, vol. 39, no. 10, Taylor & Francis, Dec. 2004, pp. 2661–70, doi:10.1081/ESE-200027022.
[28] Cheng, Jiemin, et al. “Effects of Surface-Modified Nano-Scale Carbon Black on Cu and Zn Fractionations in Contaminated Soil.” International Journal of Phytoremediation, vol. 16, Jan. 2014, doi:10.1080/15226514.2012.759530.
[29] Matlochova, Adela, et al. “The Application of Nanoscale Materials in Groundwater Remediation.” Polish Journal of Environmental Studies, vol. 22, Jan. 2013, pp. 1401–10.
[30] Asadi, M., et al. “Photocatalytic Degradation of PAHs Contaminated Soil in South Pars Economic and Energy Zone with TiO 2 Nanocatalyst.” Iranian Journal of Chemical Engineering, vol. 4, Jan. 2007.
۷- پاورقی
[1] Physical remediation
[2] Soil replacement
[3] Thermal desorption
[4]Chemical remediation
[5]Chemical leaching
[6] Chemical fixation
[7] Electrokinetic remediation
[8] Reactive sites
[9] In situ
[10] Ex situ
[11] Treatment zone
[12]Adsorption
[13] Immobilization
[14]adsorptive
[15] reactive
[16]Zero valent iron nanoparticles
[17]doping
[18]Permeable reactive barrier(PBR)
[19] Allophane
[20] Carbon black
[21]Benzene, toluene, ethylbenzene and xylene
[22]polycyclic aromatic hydrocarbons